Approfondimenti: Alla scoperta dell'atomo
Spettroscopia dei gas
Un campo di ricerca da cui emersero molte conoscenze essenziali per la comprensione della struttura atomica fu lo studio dell'emissione e dell'assorbimento della luce dai vari elementi chimici e in particolare dai gas.
La luce emessa da un gas è formata da pochi colori ben definiti, a ciascuno dei quali corrisponde uno stretto intervallo di lunghezze d'onda. Le righe dello spettro di emissione differiscono notevolmente da gas a gas, perché ogni elemento chimico emette una serie caratteristica di lunghezze d'onda.
Kirchhoff notò che la lunghezza d'onda corrispondente a ogni riga di assorbimento è uguale alla lunghezza d'onda di una delle righe luminose che appaiono nello spettro di emissione dello stesso gas. Quindi un gas può assorbire soltanto luce di lunghezza d'onda uguale a quella che emette quando è eccitato.
Lo spettro dell'idrogeno
Un'importanza particolare ebbe lo spettro dell'idrogeno, costituito da poche righe molto intense. Nel 1885, un insegnante svizzero, Johann Jakob Balmer, trovò empiricamente una semplice formula che dava le lunghezze d'onda delle linee note a quel tempo.
La formula riscritta nella sua forma più generale è:
\[\frac{1}{\lambda}=R\left(\frac{1}{2^2}-\frac{1}{n^2}\right)\]
con n = 3,4,... e dove R è la costante di Rydberg.Si scoprì poi che le righe dell'idrogeno erano più numerose e si potevano raggruppare in serie ciascuna corrispondente ad un valore fissato di n'.
Le serie sono praticamente quattro:
| n' = 1 | n = 2,3,4 | serie di Lyman (ultravioletto |
| n' = 2 | n = 3,4,5 | Serie di Balmer (visibile) |
| n' = 3 | n = 4,5,6 | serie di Paschen (infrarosso) |
| n' = 4 | n = 5,6,7 | serie di Brackett (infrarosso) |
La teoria dei quanti suggerisce un modo di interpretare tali fatti sperimentali: l'emissione o l'assorbimento di luce da parte di un atomo deve corrispondere a un aumento o, rispettivamente, a una diminuzione di energia. Dunque, se gli atomi di un dato elemento emettono soltanto luce di determinate frequenze, allora devono essere possibili soltanto variazioni di energia di determinata entità, dovute a qualche redistribuzione dei costituenti atomici.
Modello atomico di Rutherford
Una nuova ipotesi per la struttura atomica, dopo quella di Thomson, fu proposta negli anni tra il1909 e il 1911 da Ernest Rutherford, attraverso lo studio delle radiazioni emesse dalle sostanze radioattive.
In questi esperimenti, un fascio ben collimato di proiettili (particelle alfa, elettroni, raggi X, ecc.) viene inviato sul bersaglio, che di solito è una lamina sottile o una pellicola di qualche materiale. Le particelle, urtando l'ostacolo, vengono deviate o «diffuse», in seguito all'interazione con gli atomi del bersaglio; quindi, esaminando il loro moto dopo l'urto, si possono ricavare informazioni sulle proprietà delle particelle incidenti, degli atomi bombardati, o dell'interazione reciproca tra atomi e particelle.
Egli mostrò che la parte pesante e carica positivamente dell'atomo costituiva un nucleo centrale con un raggio dell'ordine di 10-12 cm e con attorno gli elettroni su orbite con raggio dell'ordine di 10-8 cm.
Nonostante ciò il modello di Rutherford presentava delle difficoltà di carattere teorico e faceva previsioni in contrasto con precisi fatti sperimentali
In primo luogo, secondo l'elettrodinamica classica, una particella carica in moto accelerato irraggia onde elettromagnetiche perdendo progressivamente energia fino a cadere sul nucleo. In secondo luogo, poiché le frequenze emesse devono essere uguali alle frequenze di rivoluzione degli elettroni, gli atomi avrebbero dovuto emettere uno spettro continuo di radiazioni e non delle semplici righe.
I postulati della teoria di Bohr
Nel 1912 - 13, per superare tali difficoltà Bohr, un fisico danese appena laureato, introdusse le seguenti ipotesi:
- per gli elettroni di un atomo esistono orbite privilegiate stabili sulle quali l'elettrone non irraggia; tali orbite sono discrete e quindi discreti sono i valori dell'energia ad esse associati (livelli energetici)
- l'irraggiamento (o l'assorbimento) di radiazione avviene per effetto della transizione di un elettrone da un'orbita a un'altra di energia inferiore (o superiore); in tale processo si ha emissione (o assorbimento) di un singolo quanto.
Regole di quantizzazione
La forza elettrica tra un elettrone di carica qe e il nucleo di carica qe (caso idrogeno) è:
\[F_{el}=k\frac{q_eq_e}{r^2}\]
Se l'elettrone si muove in un'orbita circolare stabile di raggio r attorno al nucleo e con velocità costante v, allora la forza centripeta uguaglia quella elettrica:
\[m\frac{v^2}{r} = k \frac{q_e^2}{r^2}\Rightarrow mvr=n\frac{h}{2\pi}\]
dove mvr: momento angolare, : costante di Planck, n : numero quantico
Da tali relazioni è possibile indicare i raggi dei vari livelli energetici:
\[r_n = \frac{n^2h^2}{4\pi^2kmq_e^2}\]
Attraverso il modello dell'atomo di Bohr fu possibile inquadrare teoricamente e riottenere le formule che sintetizzavano le serie spettrali dell'idrogeno. Bohr portò avanti un'analisi completa del sistema periodico degli elementi. Come risultato, nel 1921, propose un nuovo modo di rappresentare la tavola periodica degli elementi, introducendo gli elettroni che componevano i vari atomi nei vari livelli energetici.
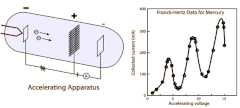
Verifica dei livelli - Esperimento di Franck e Hertz
Il concetto fondamentale di livello energetico discontinuo ha avuto una conferma sperimentale diretta grazie ad una serie di esperimenti di Franck e Hertz.
L'esperimento consisteva nello sparare elettroni entro un tubo a vuoto contenente vapori di mercurio e nel determinare l'energia perduta dagli elettroni negli urti con gli atomi e l'energia acquistata dagli atomi in questi urti: l'unico modo in cui gli elettroni potevano perdere energia era negli urti con gli atomi di mercurio.
Franck e Hertz trovarono che, finché l'energia cinetica degli elettroni prima dell'urto era bassa, per esempio pochi eV, essi conservavano quasi tutta la loro energia.
Questo risultato poteva essere spiegato così. La massa di un atomo di mercurio è più di centomila volte maggiore di quella di un elettrone; se la sua energia cinetica è bassa, l'elettrone rimbalza. Urti di questo tipo si dicono «elastici» e in un urto elastico l'energia cinetica totale del sistema si conserva.
Quando però l'energia degli elettroni venne portata a 5 eV, l'elettrone perdeva nell'urto esattamente 4,9 eV di energia. Continuando ad aumentare l'energia cinetica iniziale degli elettroni fino a 6 eV, per esempio, l'elettrone continuava a perdere 4,9 eV nell'urto con un atomo di mercurio, restando perciò con un'energia di 1,1 eV.
Questi risultati indicavano che un atomo di mercurio non può assorbire una quantità di energia inferiore a 4,9 eV e che non può assorbirne un po' di più, anche quando è disponibile.
Tale risultato, con valori energetici diversi, si ottenne ancora aumentando l'energia iniziale degli elettroni, mettendo in evidenza l'esistenza dei livelli energetici cercati. Ripetendo tale verifica con atomi diversi, si osservò una distribuzione discreta dei livelli energetici e ogni volta la quantità di energia assorbita dall'atomo in una collisione poté essere posta in relazione con righe note del suo spettro. Questa verifica sperimentale fu considerata una conferma probante della validità della teoria di Bohr.
Limiti della teoria
La teoria di Bohr, nonostante i successi, si dimostrò inadeguata per i seguenti motivi:
- non spiegava gli spettri di atomi con due o più elettroni esterni;
- non spiegava in modo quantitativo la comparsa di ulteriori righe, o la suddivisione di una riga in numerose in presenza di un campo elettrico o magnetico;
- non indicava come calcolare la probabilità di transizione tra lo stato iniziale e quello finale
- alcune previsioni non potevano essere sottoposte a verifica sperimentale in alcun modo (questo è il caso del moto degli elettroni sulle orbite).
All'inizio degli anni '20 i fisici, e lo stesso Bohr, cominciarono a lavorare seriamente alla revisione delle idee fondamentali della teoria. Il fatto più rilevante era che alla base ci fosse una «sovrapposizione» di concetti classici e di concetti quantistici. Una nuova teoria doveva dunque basarsi in modo più coerente sui concetti quantistici.